前言
製藥產業現況及CRO簡介
新藥的研究與開發是一件耗資大、時間長、風險高的事業,平均來說,將一個化合物開發成新藥的時間大約需要15年的時間,耗資3億美元,而由於藥物開發必須要和專利保護時間賽跑,因此縮短藥物開發時間顯得格外的重要,新藥能提早一天上市,就能爭取上市後多一天的專利保護時間,更可提早一天獲得營收,因此製藥市場有一個說法,藥物延緩一天上市,公司損失的金額約100萬美元,因此提高新藥開發效率、縮短新藥開發時間是各個藥廠當前的重要任務,一般藥廠在資金的壓力下,提高新藥開發效率更是刻不容緩。一般來說,中小型資源有限的生技公司提高新藥開發效率有兩種方式,一是透過大藥廠的合併,運用大藥廠的資源提高新藥開發效率,另一則是採用策略聯盟或委外研究,以較細的分工來達到提高新藥開發效率。
除了新藥開發外,一般的生技公司的在資金有限下亦無法負擔藥物製造及行銷的費用,因此,虛擬整合性藥廠的經濟模式普遍存在於製藥產業,虛擬整合性藥廠是透過策略聯盟或是委外合作等方式來完成新藥研究到行銷的程序(如圖一),而其組成包括了研究機構、生技公司、CRO(Contract
Research Organization)、CMO(Contract Manufacturing Organization)、CSO(Contract
Sales Organization)及大藥廠。
圖一:虛擬整合性藥廠簡示圖
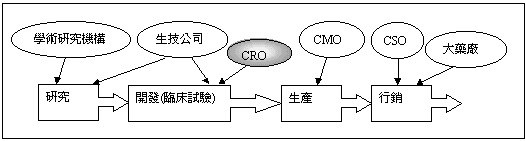
寶來研發部整理繪圖
根據統計,臨床試驗所需的經費在新藥研發過程中所佔的比例最大(圖二),所花費的時間也最長(圖三),因此臨床試驗在新藥研發的過程中扮演相當重要的角色。臨床試驗包含了計劃的管理、病人來源的取得、病人狀況的追蹤、醫院關係的維繫、資料的統計及法規的了解等,為高專業、高資金、長時間的開發過程,CRO即是接受藥廠委託而提供臨床試驗服務的機構。CRO專業的臨床試驗服務,可有效增加新藥開發效率及降低成本,12年來新藥開發的時間開始縮短,CRO的導入功不可沒,也因此臨床試驗委外的趨勢逐年增加。根據Frost
&
Sullivan估計,CRO產業的年度營收,在1998年超過46億美元,並以20%的年成長率增加,而大型CRO公司的營收,甚至有45%的成長率。
圖二:新藥開發各程序花費所佔比率
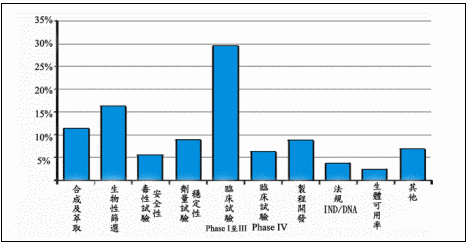
資料來源:http://www.tekes.fi(1999),寶來研發部整理
圖三:新藥開發時程及通過率
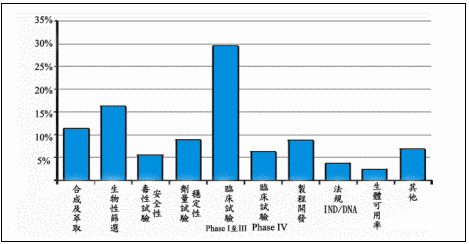
資料來源:http://www.tekes.fi,寶來研發部整理
目前台灣所進行新藥的臨床試驗約可分為四種(表一),而未來中草藥及健康食品在臨床試驗在相關法規訂定完成後,市場規模預計將還會有爆炸性的成長。
表一:台灣新藥的臨床試驗分類
|
類別 |
說明 |
台灣市場預估值 |
|
Global Regional IND Clinical Trial |
全球性新藥臨床試驗,主要資料以送審美國FDA為主,因臨床試驗地區涵蓋廣,約有40%的案件會委託給CRO
公司。 |
9000萬?2.5億 |
|
Local Registration Trial |
台灣地區區域性的臨床試驗,此類的新藥僅是為了通過國內衛生署的審查以取得許可證,估計約有40%的案件會委託給CRO公司。 |
3000萬?6000萬 |
|
Listing Trial |
國內醫學中心在進新藥之前須於該中心進行臨床試驗,估計有20%此類的案件會委託給CRO公司。 |
1000萬?6000萬 |
|
Academic Clinical Trial |
學術機構學術研究的臨床試驗,估計有15%此類的案件會委託給CRO公司。 |
數百萬 |
資料來源:國際精鼎,寶來研發部整理
研究重點
壹、公司沿革與簡介
在1999年3月底,劉致顯博士帶領著來自於健亞生技的臨床試驗服務部門的15名成員,創立了國際精鼎。董事長劉致顯博士為生物統計及電腦資訊背景出身,曾任職於美國Amgen公司資料分析部門經理及台灣健亞副總,有豐富臨床試驗服務經驗。國際精鼎擁有統計、藥學、分生、毒理、法規等專業人才,公司有80%以上員工為大學以上學歷。
由於亞洲市場逐漸被各大藥廠所重視,國際精鼎以地利之便積極於亞太地區佈局,在台灣及韓國正式設立公司(韓國公司為中韓合資,國際精鼎為大股東),並在香港、泰國、印尼、中國大陸及日本設有辦事處,且在新加坡、馬來西亞等地臨床試驗機構派有工作人員,未來並計畫在澳洲及美國設立辦事處,朝向成為亞太臨床試驗服務中心前進。
國際精鼎於公司成立時資本額為8000萬,2000年10月現金增資1.19億,現今公司實收資本1.99億,其中員工持股約佔40%,預計將於2002年掛牌。
表二:國際精鼎基本資料表
|
預定掛牌時間:2002年 |
成立時間:1999年3月 |
|
輔導券商:大華證券 |
CEO:劉致顯 博士 |
|
員工人數:65 |
資本額:1.99億 |
|
地址:台北市忠孝東路5段510號3樓 |
電話:(02)2727-1100傳真:(02)2346-5211 |
|
網址:www.apex-cro.com |
股東結構:龍慶鋼鐵、誠信創投、華岡、衛理投顧、華聯創投 |
|
產品項目:臨床試驗相關服務及相關計劃撰寫 |
策略聯盟:
Pharmaceutical Product Development(美)Harrison
Clinical Research(德)
Applied Logic Associates,
Inc.(美)
MedTrials(美) |
貳、業務簡介
目前國際精鼎提供的服務可分為兩類:新藥開發服務(臨床前動物試驗及臨床人體試驗)及生技計畫顧問(專案計畫撰寫)
一、新藥開發服務:
國際精鼎提供的新藥開發服務可由圖四簡示。
圖四:國際精鼎新藥開發服務流程
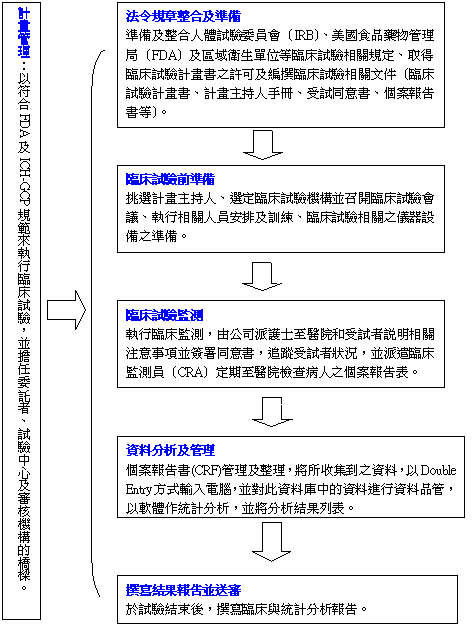
資料來源:國際精鼎,寶來研發部整理
二、生技計畫顧問:
由於國際精鼎擁有法規、生技及管理專業人才,因此也提供生技顧問服務,協助客戶計畫(如科專計畫)撰寫諮詢服務。
臨床試驗服務收費方式有兩種,一是採契訂階段性收費,較無倒帳及不必承擔藥品開發失敗風險;另一則是採共同開發原則,在藥物開發達到一定進度後(milestone)抽取一定比例的費用或權利金,此種計費可分享新藥開發成功的高獲利。目前國際精鼎擁有34個藥廠及生技公司客戶,大多分布在美國、歐洲、亞太地區(包括台灣、日本及澳洲),其中歐美客戶佔了約80%、日本客戶佔了約10%、台灣及其他地區佔了約10%。2000年完成了約80件的委託案,目前有76個委託案分布在七個國家進行,而有超過60%的營收來自於跨國新藥開發委託案。
參、財務狀況
由於國際精鼎目前為未公開發行之公司,因此財務狀況並未公開,公司透露1999年及2000年皆處虧損狀態,但虧損逐年減少,公司預計2001年至少達到損益兩平。
肆、合作對象
一、臨床試驗中心:
國際精鼎與國內多所臨床試驗醫學機構(包括台大、奇美醫院等)皆有合作關係,與美國SRI(Southern Research
Institute,主要從事動物試驗)也保持密切合作。
二、ClinTrust Global Alliance:
國際精鼎除了積極在亞太地區成立公司及辦事處外,在歐洲則與Harrison Clinical Research(德)、Applied Logic
Associates, Inc.(美)及MedTrials(美)結盟,共同成立ClinTrust Global
Alliance。透過此結盟可以結合北美、歐洲及亞洲三地的CRO資源,提供全球臨床試驗服務。成員公司若承接委託案的臨床試驗地區非屬公司掌握區域,則會將計劃轉介給所在區域的其他成員公司,經由在地CRO公司對當地文化及法規的精確掌握,提供更完善的服務。此外,此結盟還可以促進公司經驗交流及提供全球性的員工訓練。
三、PPD:
國際精鼎與全球第四大CRO公司Pharmaceutical Product
Development(PPD)策略聯盟,共同開發亞洲臨床試驗服務市場,目前已有一跨國性委託案正在洽談中,若能取得此委託案,預計將為國際精鼎帶來可觀的獲利。
伍、競爭對象
由於國際精鼎以亞太為主要市場,在台灣主要的競爭對象如表二,其中維州、晉加、佳生及健亞為台灣本土廠商,國際精鼎相較於這些本土公司有規模大、高專業度及國際化等競爭優勢。而全球第一大CRO昆泰(Quintiles
Transnational Corp.)在台灣有設立分公司,全球第二大CRO科文斯(Covance
Inc.)與經濟部有合作關係,這兩大公司想進軍亞太地區訊息非常濃厚,算是國際精鼎在亞太地區主要的假想敵,雖然國際精鼎在台灣是CRO龍頭公司,但在台灣之外的亞太市場誰勝誰負尚難定論。在亞太地區,國際精鼎有地理文化上的優勢,雖全球規模比不上昆泰與科文斯,但國際精鼎積極尋求與全球第四大CRO公司PPD策略聯盟,彌補在規模上的不足,與全球前兩大CRO公司於亞太戰場競爭。
表二:國際精鼎在台灣競爭對象
|
公司名稱 |
資本額 |
網址 |
|
維州生物科技股份有限公司 |
500萬 |
www.vcro.com.tw |
|
晉加股份有限公司 |
1000萬 |
www.statplusinc.com |
|
佳生科技顧問股份有限公司 |
5000萬 |
www.protechcro.com.tw |
|
健亞生物科技股份有限公司 |
8.75億 |
www.genelabs.com.tw |
|
昆泰(Quintiles Transnational) |
25.7億美元(市值) |
www.quintiles.com |
|
科文斯(Covance) |
11.5億美元(市值) |
www.covance.com |
資料來源:經濟部商業司,yahoo.finance,寶來研發部整理
陸、SWOT分析
Strength:
- 臨床試驗程序符合ICH-GCP(國際醫藥法規協合會-藥品優良臨床試驗規範),並擁有專業、經驗豐富的人力素質。
- 員工流動率低、向心力強。
- 公司經營主動積極,亞太地區佈局廣。
- 目前為台灣第一大CRO公司,擁有與國外策略聯盟洽談的條件。
Weakness:
- 規模遠小於全球前五大CRO公司,需以策略聯盟才有較大機會爭取全球性的案子。
- 在台灣之外的亞太地區雖有據點,但皆屬小型規模。
Opportunity:
- 為增加新藥開發效率及降低成本,生技公司從事研究,CRO負責發展(臨床試驗)已成趨勢,CRO產業的成長可期。
- 跨國性臨床試驗案件持續成長,帶動亞太地區臨床試驗,本土CRO公司因地理位置及文化較歐美CRO具優勢,重要性將日益增加。
Threat:
- CRO合併及策略聯盟所產生的效應不可忽視,將來其他亞太地區的CRO公司的合併或策略聯盟可說是最大的威脅。
- 大陸市場為亞太地區之重要市場,將來大陸CRO公司的威脅不可輕忽。
- 亞太地區仍有許多國家相關法規仍不盡完善,或民眾接受臨床試驗意願不高,臨床試驗的發展將不若歐美地區成熟。
- 藥廠及生技公司合併所產生的縮減臨床試驗委託案效應是否繼續發生,將影響CRO產業的發展。
結論
- 為了產生更高效率及有效降低成本,各大藥廠及生技公司委外研發新藥已成趨勢,根據Tekes公司指出,在2000年,委外研發計劃約佔總研發計劃50%,在2005年預計更可達到65%,加上製藥研發經費仍以每年約14%的成長率增加,在這個趨勢下,CRO將是最直接受惠的產業。
- CRO相較於其他生技產業的風險來得低,但卻較其他生技產業的獲利快,因此想投資生技產業又害怕高風險的投資者,CRO公司不啻為適當的投資標的。
- 國際精鼎擁有提供符合ICH-GCP臨床試驗服務的專業團隊及豐富經驗,公司創立初期隨即取得不少契約,加上積極佈局亞太地區,尋求策略聯盟夥伴,短期之間已成為台灣第一大CRO公司,為進軍國際市場站穩了腳步。國際精鼎若能在積極拓展業務來源之外,保有提供服務的專業性以建立口碑形象,朝向「服務深度自我研發,服務廣度尋求策略聯盟」的方向前進,要成為亞太地區臨床試驗服務中心應是指日可待。